L’Institut de la Màcula, primer centre acreditat a Europa per dur a terme l’assaig mèdic CHROMA
02/02/2015 ·
La Degeneració Macular Associada a l’Edat (DMAE) en la seva variant seca o atròfica és la primera causa de ceguesa no-evitable en el món en persones majors de 50 anys. Lampalizumab és la primera teràpia que mostra eficàcia significativa frenant la progressió de la DMAE, especialment en pacients amb unes característiques genètiques determinades. L’estudi, liderat per la farmacèutica Roche i ja en fase de reclutament, converteix a l’Institut de la Màcula en un centre líder en assaigs clínics.
L’assaig en fase III avalua l’eficàcia i la seguretat de lampalizumab administrat amb injeccions intrevítrees a pacients amb atròfia geogràfica (AG) secundària a Degeneració Macular Associada a l’Edat (DMAE). Els estudis també determinaran si els pacients amb un determinat biomarcador –una mutació del factor I– es poden beneficiar més del tractament amb Lampalizumab.
Aquests assaigs de fase III, anomenats Chroma (GX29176) i Spectri (GX29185), són estudis aleatoris amb un disseny idèntic, amb doble emmascarament, que comparen una dosi de 10 mg de Lampalizumab administrada cada 4 o 6 setmanes mitjançant injeccions intravítrees simulades. En cada estudi es reclutaran aproximadament 936 pacients (188 pacients amb biomarcador positiu i 124 amb biomarcador negatiu en cada un dels grups: tractament simulat, Lampalizumab cada 4 setmanes [c4s] i Lampalizumab cada 6 setmanes [c6s] de cada estudi). Els estudis reclutaran pacients d’aproximadament 300 centres d’investigació de 24 països de tot el món. Els criteris d’inclusió principals són similars als de l’estudi MAHALO de fase II i inclouen la presència d’atròfia geogràfica (AG) als dos ulls sense antecedents de DMAE neovascular (humida).
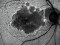
L’objectiu principal dels estudis és demostrar una reducció en la taxa de progressió de l’Atròfia Geogràfica. Aquest criteri de valoració de l’eficàcia, avaluat al cap d’un any (setmana 48) es defineix com la mitjana de la variació a l’àrea de lesió d’AG de l’ull de l’estudi triat des del moment basal, mesurat per autofluorescència de l’ull (AFO), una tècnica d’imatge utilitzada per a proporcionar informació sobre la mida i el tipus de lesions d’AG en la màcula. Els objectius secundaris dels estudis, planificats per a l’avaluació als dos anys (96 setmanes), es centren en l’avaluació de l’impacte del tractament amb Lampalizumab sobre la funció visual dels pacients. Si els estudis es completen amb èxit, està previst el seguiment a llarg termini dels pacients que completin Chroma i Spectri a través d’un estudi d’extensió obert posterior.
Els resultats positius d’eficàcia i seguretat de l’assaig de fase II previ, l’estudi MAHALO, recolzen aquests assaigs de fase II. El criteri de valoració principal de l’estudi MAHALO mostrava una reducció del 20% al mes 18 en la progressió de la lesió d’AG en pacients tractats mensualment amb Lampalizumab en comparació amb el tractament simulat. A més, les dades d’una subpoblació de pacients amb AG que rebien mensualment Lampalizumab i eren positius per al biomarcador factor del complement I (CFI), van demostrar una reducció del 44% de la taxa de progressió de la malaltia als 18 mesos.
“Lampalizumab és una fita en la lluita contra la DMAE atròfica. Per primera vegada un medicament ha demostrat l’eficàcia en un estudi de Fase II per a reduir la progressió del deteriorament. La Fase III és una oportunitat per als pacients que tenen la possibilitat de millorar la degeneració. Els resultats d’aquests assaigs de Fase III poden confirmar aquests resultats prometedors”, va assenyalar el Dr. Jordi Monés, oftalmòleg especialista en màcula, retina i vitri de l’Institut de la Màcula i un dels principals investigadors d’aquests assaigs de Fase III.